teori atom – Tentu kalian sudah mengetahui materi yang kita bahas kali ini. Karena, materi teori atom ini pasti sering kamu jumpai di mata pelajaran fisika. Bahan ini tentunya juga bukan bahan yang sederhana. Nah, pada pembahasan kali ini kita akan membahas teori atom menurut para ahli beserta gambarannya.
Sebelum kita membahas materi teori atom menurut para ahli, kita harus mengetahui terlebih dahulu tentang pengertian dan asal usul teori atom. Kata atom berasal dari kata “atom” dalam bahasa Yunani yang berarti “tak terpisahkan”.
Awal mula teori dasar atom dibuat oleh seorang ahli dari Yunani, yaitu Democritus pada abad ke-4 SM. Menurut teori atom yang dikemukakan oleh Democritus, atom adalah benda yang sangat kecil sehingga tidak dapat dibagi lagi.
Menurutnya, atom benar-benar padat, ada ruang kosong di antara atom untuk memberi ruang bagi pergerakannya (seperti di air dan udara), dan tidak memiliki struktur internal.
Namun, model teori atom Democritus tidak memiliki bukti eksperimental sampai teori baru muncul pada tahun 1800-an berdasarkan hasil eksperimen. Beberapa teori atom yang muncul dan banyak dikenal dalam ilmu fisika saat ini adalah teori atom menurut Rutherford, John Dalton, dan JJ. Thomson.
Contents
teori atom John Dalton
Pada tahun 1803, John Dalton mengajukan teori atom berdasarkan dua hukum, yaitu hukum komposisi tetap (hukum Prout) dan hukum kekekalan massa (hukum Lavoisier).
Menurut Prouts: “Perbandingan massa unsur-unsur dalam suatu senyawa selalu tetap.”
Menurut Lavosier: “Massa total zat sebelum reaksi akan selalu sama dengan massa total produk reaksi”.
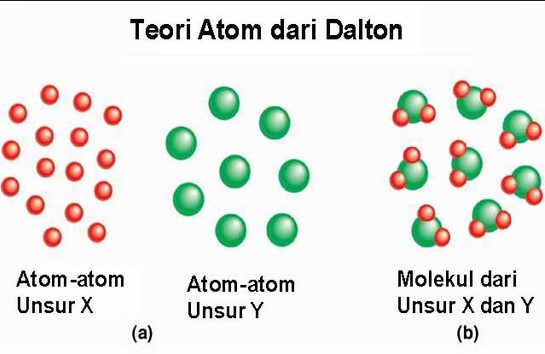
 Berdasarkan kedua hukum tersebut, John Dalton mengungkapkan pandangannya tentang teori atom sebagai berikut:
Berdasarkan kedua hukum tersebut, John Dalton mengungkapkan pandangannya tentang teori atom sebagai berikut:
- Atom adalah bagian terkecil dari materi yang tidak dapat dibagi lagi.
- Atom digambarkan sebagai bola padat yang memiliki ukuran sangat kecil.
- Atom bergabung membentuk senyawa. Misalnya, air terdiri dari atom hidrogen dan atom oksigen.
Reaksi kimia adalah pemisahan atau penataan ulang atom-atom sehingga atom-atom tersebut tidak dapat diciptakan atau dimusnahkan.
Kelebihan:
Mulai membangkitkan minat dalam penelitian tentang model atom.
Kelemahan:
Teori atom menurut Dalton tidak dapat menjelaskan bahwa larutan dapat menghantarkan arus listrik.
Baca juga:
Model teori atom JJ. Thomson
Menurut JJ Thomson pada tahun 1900, menurutnya di dalam atom terdapat partikel elektron dan proton. Berdasarkan hasil eksperimennya, proton memiliki massa yang lebih besar daripada elektron, sehingga model atom Thomson dapat digambarkan sebagai proton tunggal yang besar.
Proton memiliki elektron yang menetralkan muatan positif pada proton. Menurut JJ. Thomson, atom terdiri dari bola bermuatan positif yang dikemas rapat. Secara umum, teori atom Thomson berbunyi: “Atom adalah bola padat yang bermuatan positif dan di dalamnya muatan negatif elektron tersebar.”
 Secara sederhana, model teori atom Thomson dapat dianalogikan seperti jambu biji yang telah dikupas kulitnya. Nah, biji jambu biji yang tersebar merata dimodelkan sebagai elektron, sedangkan bola daging jambu biji padat dianalogikan sebagai proton.
Secara sederhana, model teori atom Thomson dapat dianalogikan seperti jambu biji yang telah dikupas kulitnya. Nah, biji jambu biji yang tersebar merata dimodelkan sebagai elektron, sedangkan bola daging jambu biji padat dianalogikan sebagai proton.
Kelebihan:
Teori atom Thomshon mampu membuktikan bahwa ada partikel bermuatan negatif lainnya dalam atom. Artinya atom bukanlah bagian terkecil dari suatu unsur.
Kelemahan:
Model Thomson tidak dapat menjelaskan komposisi muatan negatif dan positif dalam bidang atom.
model atom Rutherford
Menurut Rutherford, pada tahun 1910, bersama dua orang muridnya (Hans Geiger dan Erners Masreden), ia melakukan percobaan yang dikenal dengan hamburan sinar alfa (λ) pada lempengan emas tipis. Dari pengamatannya diketahui bahwa sebagian besar partikel alfa dapat menembus lempengan emas tanpa dibelokkan.
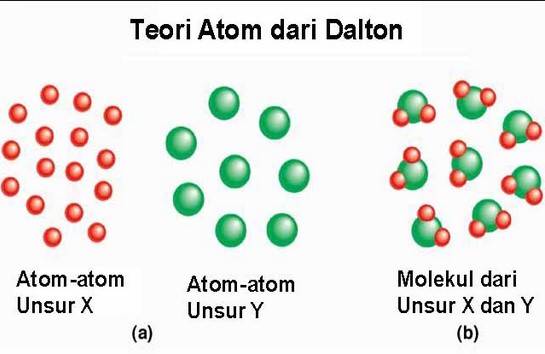
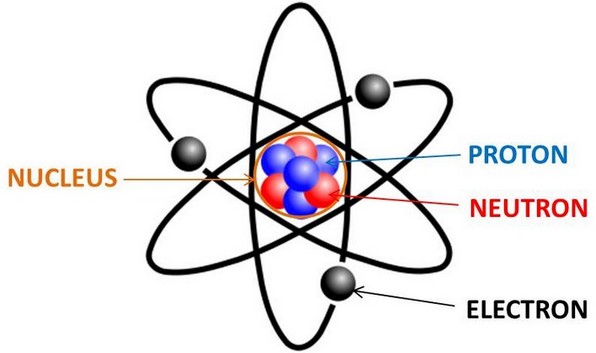 Berdasarkan gejala yang terjadi, Rutherford menyimpulkan bahwa:
Berdasarkan gejala yang terjadi, Rutherford menyimpulkan bahwa:
- Atom bukanlah bola padat, karena hampir semua partikel alfa ditransmisikan.
- Jika lempengan emas dianggap sebagai lapisan atom emas, maka di dalam atom emas terdapat partikel-partikel kecil yang bersifat positif.
- Partikel-partikel ini adalah partikel-partikel yang menyusun inti atom.
Berdasarkan pengamatan tersebut, Rutherford mengusulkan suatu model atom, yaitu “Sebuah atom terdiri dari inti atom yang sangat kecil, yang bermuatan positif, dan dikelilingi oleh elektron yang bermuatan negatif”.
Kelebihan:
Atom terdiri dari inti dan elektron yang mengelilingi inti.
Kelemahan:
Teori ini tidak dapat menjelaskan mengapa sebuah elektron tidak dapat jatuh ke dalam inti.
Model atom Niels Bohr
Setelah Neils Bohr pada tahun 1913, dia mengoreksi kesalahan atom Rutherford melalui eksperimennya pada spektrum atom hidrogen. Berdasarkan hasil eksperimennya, Bohr memberikan gambaran tentang keadaan orbit elektron dan pendudukan daerah sekitar inti atom. Menurut Neils Bohr, elektron hanya mengelilingi inti atom pada orbit tertentu, yaitu hanya ada sejumlah orbit tertentu dan perbedaan antara orbit tersebut adalah jarak dari orbit ke inti atom.
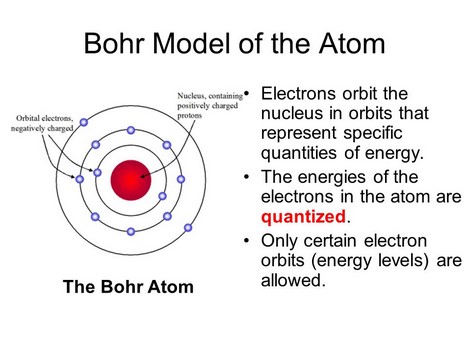 Penjelasan Niels Bohr tentang atom merupakan gabungan dari teori klasik Planck dan teori kuantum Rutherford. Secara umum, Niels Bohr menyajikan model atom sebagai berikut:
Penjelasan Niels Bohr tentang atom merupakan gabungan dari teori klasik Planck dan teori kuantum Rutherford. Secara umum, Niels Bohr menyajikan model atom sebagai berikut:
- Elektron dan atom bergerak mengelilingi inti dengan cara tertentu, dan tidak memancarkan energi.
- Elektron dan atom dapat bergerak di antara jalur.
- Pergerakan elektron dalam atom dari tingkat energi tertinggi ke tingkat terendah disertai dengan pancaran energi.
Menurut model teori atom Bohr, elektron berputar mengelilingi inti dalam orbit tertentu yang dikenal sebagai tingkat energi atau kulit elektron. Tingkat energi terendah adalah kulit elektron yang terletak di bagian terdalam, semakin jauh ke luar, semakin banyak jumlah kulit elektron dan semakin tinggi tingkat energinya.
Kelebihan:
Atom Bohr adalah atom yang terdiri dari beberapa kulit sebagai tempat pergerakan elektron.
Kelemahan:
Model atom ini tidak dapat menjelaskan efek Strack dan efek Zeeman.
Nah, itulah penjelasan teori atom menurut para ahli dan gambar yang bisa kami berikan. Setelah Anda memahami materi ini, Anda dapat melanjutkan ke materi berikutnya yaitu Struktur atom. Terima kasih telah berkunjung dan semoga bermanfaat.
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa