Rumusrumus.com kali ini akan membahas tentang sifat rumus koligatif Solusi, juga akan menjelaskan memahami lebih sifat koligatif Solusi dengan Informasi miliknya
Contents
memahami
Sifat koligatif
Sifat koligatif adalah sifat fisik larutan yang bergantung pada konsentrasi partikel larutan, tetapi tidak bergantung pada jenisnya. Larutan elektrolit memiliki sifat koligatif yang lebih besar daripada larutan non-elektrolit dengan konsentrasi yang sama karena larutan elektrolit memiliki jumlah partikel terlarut yang lebih banyak.
Tekanan uap larutan
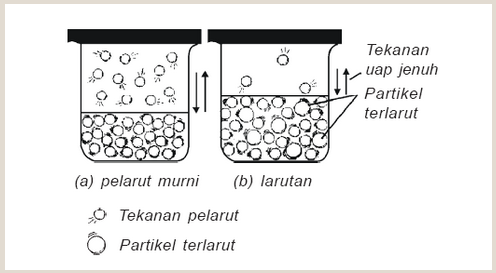
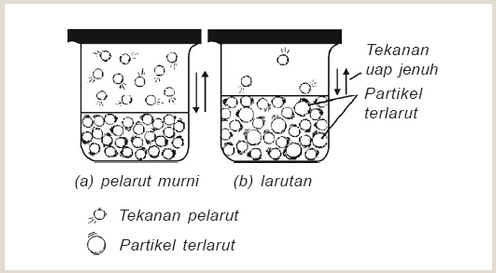
Tekanan uap suatu zat adalah tekanan yang diberikan pada uap jenuh zat itu. Semakin tinggi suhu, semakin besar tekanan uapnya. Jika larutan tidak menguap, tekanan uap larutan akan lebih rendah dari tekanan uap pelarut. Perbedaan antara tekanan uap pelarut murni dan tekanan uap larutan disebut penurunan tekanan uap larutan
ΔP = P0 – P
Menurut Roulth, bila larutan tidak menguap maka penurunan tekanan uap larutan sebanding dengan fraksi mol zat terlarut, sedangkan tekanan uap larutan sebanding dengan fraksi mol pelarut.
P = Xpel x P0
ΔP = Xter x P0
Larutan menurunkan tekanan uap pelarut.
Rumus sifat koligatif larutan memiliki delapan rumus yang terbagi menjadi empat rumus sifat koligatif larutan non-elektrolit dan empat rumus sifat koligatif larutan elektrolit.
Rumus sifat koligatif larutan elektrolit
1. ΔP (penurunan tekanan uap jenuh)
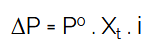
Informasi:
- ΔP = tekanan uap jenuh
- P° = tekanan uap pelarut murni
- X† = fraksi mol pelarut
- i = faktor van’t hoff
2. Tinggi titik didih
![]()
Informasi:
- ΔTb = tinggi titik didih
- Kb = tetapan tinggi titik didih
- m = molalitas larutan
- i = faktor van’t hoff
3. Depresi titik beku
![]()
Informasi:
- ΔTf = penurunan titik beku
- Kf = tetapan penurunan titik beku
- m = molalitas larutan
- i = faktor van’t hoff
4. Tekanan osmosis larutan
![]()
Informasi:
- ∏ = tekanan osmotik larutan
- M = molaritas
- R = konstanta gas
- T = suhu mutlak
- i = faktor van’t hoff
Rumus sifat koligatif larutan non-elektrolit
1. Penurunan tekanan uap jenuh
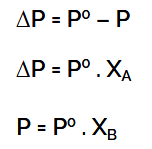 informasi;
informasi;
- ΔP = penurunan tekanan uap jenuh
- P° = tekanan uap pelarut murni
- XA = fraksi mol pelarut
- XB = fraksi mol pelarut
2. Tinggi titik didih
![]()
Informasi:
- ΔTb = tinggi titik didih
- Kb = tetapan tinggi titik didih
- m = molalitas larutan
3. Depresi titik beku
![]()
Informasi:
- ΔTf = penurunan titik beku
- Kf = tetapan penurunan titik beku
- m = molalitas
4. Tekanan osmotik
![]()
Informasi:
- ∏ = tekanan osmotik larutan
- M = molaritas
- R = konstanta gas
- T = suhu mutlak
Kesimpulan:
Penurunan titik beku umumnya memiliki konsep yang sama dengan peningkatan titik didih. Larutan yang titik bekunya lebih rendah dari pada pelarutnya. Semakin tinggi konsentrasi larutan, semakin rendah titik beku larutan. Penurunan titik beku larutan dapat dicari dengan menggunakan rumus ΔTf = mxKf, dimana ΔTf adalah penurunan titik beku, m adalah molalitas larutan, dan Kf adalah tetapan penurunan titik beku untuk molalitas.
Ketinggian titik didih suatu larutan selalu memiliki nilai yang lebih tinggi daripada titik didih pelarut murni. Ini karena partikel dalam larutan mencegah penguapan partikel pelarut. Tinggi titik didih dapat diukur dengan Rumus ΔTb = m.Kbdimana ΔTb adalah tinggi titik didih, Kb adalah tetapan tinggi titik didih, am adalah molalitas.
Baca juga:
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa