Rumusrumus.com kali ini akan membahas tentang kimia pecahan kalitidak hanya rumus fraksi mol, tetapi akan menjelaskan tentang Pengertian fraksi molserta hubungan antara molaritas dan molaritas dan juga menjelaskan tentang hubungan molalitas dengan persen massa secara terperinci. Selain itu, juga akan dijelaskan maknanya normalitas bersama dengan rumus normalitas
Contents
Definisi fraksi mol
Fraksi mol adalah ukuran konsentrasi larutan yang menyatakan rasio berkali-kali Bagian dari zat dengan jumlah total mol Komponen solusi.
pecahan kali juga sering disebut fraksi jumlah dan selalu identik dengan bilangan pecahan, yang dinyatakan sebagai jumlah molekul suatu komponen dibagi dengan jumlah total molekul. Konsep ini hanyalah salah satu cara untuk menunjukkan adanya komposisi campuran dengan kesatuan tanpa dimensi. Fraksi mol terkadang diwakili oleh huruf Yunani, bukan alfabet Romawi.
Dalam perhitungan Kimia jumlah zat terlarut dalam suatu pelarut disebut konsentrasi. Konsentrasi larutan harus dihitung secara tepat dengan menentukan massa zat Pelarut dan Pelarut.
Konsentrasi larutan ini adalah: molaritas, fraksi mol, molaritas Dalam persen massa. Hal-hal tersebut dijelaskan satu per satu dan dilengkapi dengan rumusnya masing-masing. mengikuti Rumusrumus.com akan menjelaskan.
Rumus fraksi mol
Molalitas adalah konsentrasi larutan yang dinyatakan berkali-kali, zat terlarut dan 1 kilogram atau 1000 gram pelarut. Rumus untuk molalitas adalah sebagai berikut:
Jumlah mol pelarut / 1Kg pelarut
pecahan kali zat terlarut (Xt) biasanya dirumuskan dengan menggunakan rumus berikut:
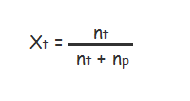
Informasi:
- Xt : fraksi mol pelarut
- Np : Jumlah mol pelarut
- Nt : Jumlah mol zat terlarut
Fraksi mol zat terlarut (Xp) biasanya diformulasikan menggunakan rumus berikut:

Hubungan antara molalitas dan persen massa
persen massa merupakan satuan konsentrasi yang juga dapat digunakan larutan kimia. Contohnya adalah larutan yang biasa kita jumpai setiap hari yaitu larutan alkohol 75% dan larutan asam asetat 24%. Persen massa adalah jumlah gram zat terlarut dalam 100 gram massa larutan.
Persamaan yang menunjukkan perhitungan persentase massa adalah sebagai berikut:
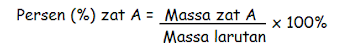
Hubungan antara molalitas dan molaritas
Molaritas menyatakan jumlah mol zat terlarut dalam satu liter larutan. Molaritas Bisa dikonversi menjadi molalitas, cara mengubah volume larutan menjadi massa larutan. Konversi dari volume ke massa membutuhkan data massa jenis larutan, yang dapat dirumuskan sebagai berikut:
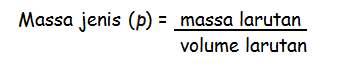
normalitas adalah besaran yang menyatakan berapa kali ekivalen zat terlarut dalam setiap satuan volume larutan. Satuan normalitas adalah normal (N) yang sama dengan mol/liter ekuivalen. Normalitas juga memiliki rumus berikut:
N = Ek/V atau N = na/V atau mungkin N = Maks
Informasi:
Eche adalah ekivalen mol, artinya jumlah mol dikalikan dengan jumlah ion H+ atau ion OH-
Sifat koligatif larutan
Meskipun alam koligatif selalu termasuk larutan yang berbeda, tetapi sifat koligatif tidak bergantung pada interaksi antara pelarut dan molekul pelarut, tetapi tergantung pada jumlah zat terlarut yang terlarut dalam suatu larutan. Sifat koligatif terdiri dari penurunan tekanan uap serta peningkatan titik didih dan penurunan titik beku, serta tekanan osmotik.
Molekul cairan meninggalkan permukaan menyebabkan tekanan uap cairan menumpuk. Semakin mudah molekul cairan berubah menjadi uap, semakin tinggi tekanan uap cairan tersebut.
Namun, ketika tekanan cairan dilepaskan pada larutan yang tidak menguap, partikel larutan mengurangi penguapan molekul cairan.
Laut Mati adalah contoh penurunan tekanan uap pelarut oleh larutan yang tidak mudah menguap.
Contoh soal pecahan mol
Untuk lebih memahami pengertian dan rumus pecahan mol, ada baiknya Anda berlatih soal-soal yang paling jitu, berikut ini contoh soal pecahan mol lengkap dengan pembahasannya.
Contoh soal 1
Suatu larutan terdiri dari 3 mol zat A, 3 mol zat B, dan 4 mol zat C. Hitunglah fraksi mol masing-masing zat tersebut?
Diskusi:
Diketahui adalah:
Resolusi:
XA = nA / (nA + nB + nC)
XA = 3 / (3 + 3 + 4)
XA = 0,3
XA = nA / (nA + nB + nC)
XA = 3 / (3 + 3 + 4)
XA = 0,3
XA = nA / (nA + nB + nC)
XA = 4 / (3 + 3 + 4)
XA = 0,4
Jadi jumlah XA + XB + XC = 0,3 + 0,3 + 0,4 = 1
Itulah pembahasan singkat materi pada rumus fraksi mol beserta contoh soalnya, semoga bermanfaat.
website Pelajaran SD SMP SMA dan Kuliah Terlengkap
mata pelajaran
jadwal mata pelajaran mata pelajaran sma jurusan ipa mata pelajaran sd mata pelajaran dalam bahasa jepang mata pelajaran kurikulum merdeka mata pelajaran dalam bahasa inggris mata pelajaran sma jurusan ips mata pelajaran sma
bahasa inggris mata pelajaran
bu ani memberikan tes ujian akhir mata pelajaran ipa
tujuan pemberian mata pelajaran pendidikan kewarganegaraan di sekolah adalah
dalam struktur kurikulum mata pelajaran mulok bersifat opsional. artinya mata pelajaran smp mata pelajaran ipa mata pelajaran bahasa indonesia mata pelajaran ips mata pelajaran bahasa inggris mata pelajaran sd kelas 1
data mengenai mata pelajaran favorit dikumpulkan melalui cara
soal semua mata pelajaran sd kelas 1 semester 2 mata pelajaran smk mata pelajaran kelas 1 sd mata pelajaran matematika mata pelajaran ujian sekolah sd 2022
bahasa arab mata pelajaran mata pelajaran jurusan ips mata pelajaran sd kelas 1 2021 mata pelajaran sbdp mata pelajaran kuliah mata pelajaran pkn
bahasa inggrisnya mata pelajaran mata pelajaran sma jurusan ipa kelas 10 mata pelajaran untuk span-ptkin mata pelajaran ppkn mata pelajaran ips sma mata pelajaran tik
nama nama mata pelajaran dalam bahasa inggris mata pelajaran pkn sd mata pelajaran mts mata pelajaran pjok
nama nama mata pelajaran dalam bahasa arab mata pelajaran bahasa inggrisnya mata pelajaran bahasa arab
seorang pengajar mata pelajaran akuntansi di sekolah berprofesi sebagai
nama mata pelajaran dalam bahasa jepang
hubungan bidang studi pendidikan kewarganegaraan dengan mata pelajaran lainnya
dalam struktur kurikulum mata pelajaran mulok bersifat opsional artinya mata pelajaran dalam bahasa arab
tujuan mata pelajaran seni rupa adalah agar siswa